Extraction of magnesium from ferronickel slag produced in the electric furnace smelting by chloridizing volatilization
-
摘要:
针对电炉冶炼红土镍矿产生的镍铁渣中镁含量高导致渣无法大宗利用及造成镁资源浪费的问题,文中提出碳共存条件下用CaCl2氯化挥发渣中MgO的技术思路。研究了氯化温度、保温时间、碳及氯化钙添加量等对渣中镁挥发率的影响。研究结果表明:在n(C)/n(Mg)=1.25、n(CaCl2)/n(Mg)=1、1 300 ℃保温120 min条件下,镍铁渣中镁的挥发率可以达到67.22%,氯化后渣中MgO含量降低至8.21%。碳共存条件下CaCl2氯化渣中镁的过程是:O2和渣中酸性氧化物使CaCl2分解产出Cl2,Cl2与MgO反应生成MgCl2,碳的作用是降低Cl2与MgO反应时的反应温度。随着氯化过程的进行,渣中主要物相由Mg2SiO4转变为CaMgSi2O6,渣的熔化性温度由最初的1 400 ℃降低至1 300 ℃。
Abstract:Aiming at the problem that the high content of magnesium in ferronickel slag produced by electric furnace smelting laterite nickel minerals leads to the inability of slag to be used in large quantities and the waste of magnesium resources, the technical idea of chlorination of MgO in volatile slag with CaCl2 under the condition of carbon coexistence was proposed. The effects of chlorination temperature, holding time, carbon and calcium chloride addition on the volatilization rate of magnesium in slag were studied. The results showed that the volatilization rate of magnesium in ferronickel slag could reach 67.22% and the content of MgO in the slag after chlorination was reduced to 8.21% when n(C)/n(Mg) = 1.25, n(CaCl2) / n(Mg) = 1, and holding at 1 300 ℃ for 120 min. The extraction process of magnesium from chlorination slag with CaCl2 under the condition of carbon coexistence was that O2 and acidic oxides in the slag made CaCl2 decompose to Cl2, and then it reacted with MgO to form MgCl2. The role of carbon was to reduce the reaction temperature of Cl2 and MgO. With the chlorination process, the main phase in the slag changed from Mg2SiO4 to CaMgSi2O6, and the melting temperature of the slag decreased from the initial 1 400 °C to 1 300 °C.
-
Keywords:
- laterite nickel ore /
- ferronickel slag /
- CaCl2 /
- carbon /
- magnesium /
- chloridzing volatilization
-
以红土镍矿为原料生产镍铁时会产出大量含镁较高的镍铁渣,将镍铁渣用作建材是其主要的资源化利用方法 [1-3],但渣中二价镁的稳定性问题导致其在建材方面使用量较少[4],大多数镍铁渣仍然在堆存。如能提取镍铁渣中的镁,既实现了镁资源的利用,又为镍铁渣的大宗利用创造条件 [5- 6]。
镍铁渣中镁的提取方法有真空热还原和水溶液浸出2种方法。真空热还原法是用Si-Fe、Si、Al等做还原剂,配入CaO,经压球后通过高温在真空下将渣中的MgO还原为金属镁[7-9]。水溶液浸出法有2种,一种是用水溶液浸出渣中镁并将其制备为镁盐[10-12];另一种是用水溶液浸出渣中的硅等杂质,使渣中镁的品位提高[13]。真空还原方法需要将镍铁冷渣、还原剂等混合后加热至1 300 ℃以上才能实现镁还原,不仅物料加热需要消耗大量热量,而且Si-Fe等还原剂属于高能耗产品,所以真空还原方法提取渣中镁的能耗较高;水溶液浸出方法尽管热耗较低,但会产生大量废水需要治理,导致整个流程的处理成本增加。需要探索能耗较低、污染物排放量小的镁提取方法。
氯化挥发法是用Cl2、NaCl、CaCl2等作为氯化剂,在高温条件下将物料中的金属氧化物转变为易挥发的金属氯化物的方法,已广泛应用于多种金属的提取[14-20]。在碳与氯化剂共存时MgO可以转变为MgCl2[21-23],尤其是,当MgO浓度较高,且温度在725 ℃以上时蒸气压可迅速升高[24]。镍铁渣放渣时渣温在1 450~1 550 ℃之间[25],如果在镍铁渣放渣时向渣中加入氯化剂和碳,可利用渣携带的热量或向渣中补入热量,以实现渣中镁的氯化挥发,随后对挥发出的MgCl2进行收集。本工艺过程的实施仅需配套MgCl2收集设备,在放渣过程中进行渣中镁的氯化挥发,不产生废水等污染物。
本文以镍铁渣为原料、CaCl2为氯化剂,在碳共存的条件下对渣中的镁进行了氯化挥发研究,在氯化热力学及氯化过程炉渣物性变化研究的基础上,探究了氯化温度、氯化时间、碳及CaCl2添加量等因素对镁挥发率的影响,研究结果为镍铁渣中镁的提取提供新的技术思路。
1 实验部分
1.1 实验原料
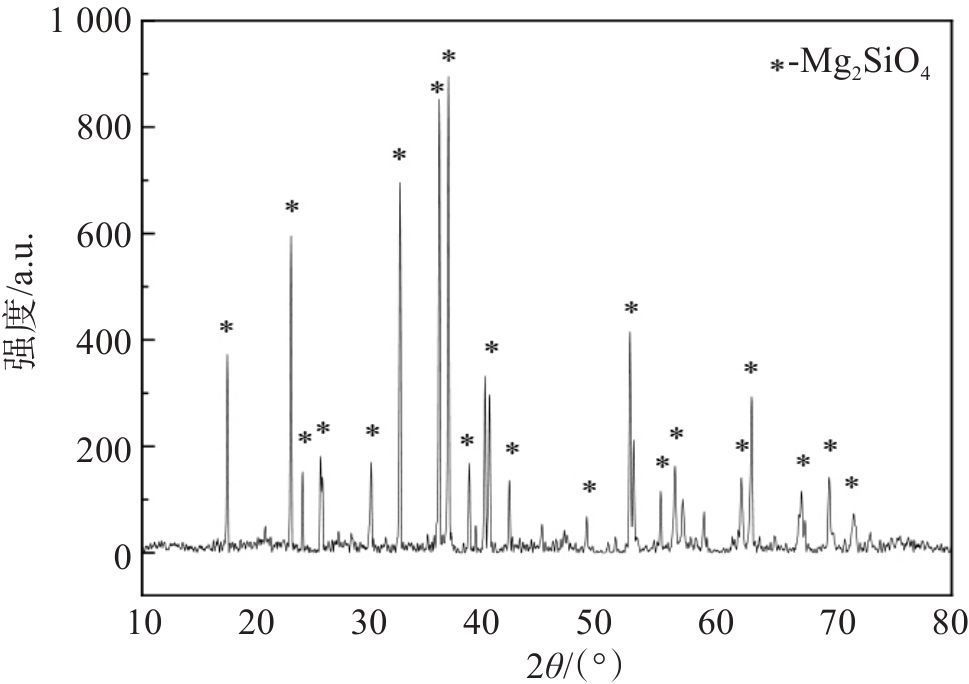
实验所采用的镍铁渣采自以红土镍矿为原料、电炉法生产镍铁过程产出的冶炼渣。冶炼渣经干燥、破碎并磨细至<75 μm占90%以上,对镍铁渣的主要组分进行检测(GB/T 1549—2008),检测结果见表1。对渣中主要物相采用X-衍射仪进行检测(布鲁克XRD D8 X射线衍射仪),物相检测结果见图1。由表1可得,镍铁渣中SiO2和MgO含量较高,属于主要组分,由图1可知,渣中MgO的物相为Mg2SiO4。
表 1 镍铁渣主要成分Table 1. Main components of ferronickel slag成分 Fe2O3 SiO2 Al2O3 MgO CaO 含量 3.26 51.92 5.63 26.31 1.82 实验使用的碳质还原剂为产自陕西榆林的粉状兰炭,经干燥后兰炭磨细至<75 μm占85%以上,兰炭主要成分见表2。无水CaCl2为市售分析纯。
表 2 兰炭主要成分Table 2. Main components of semi-coke成分 Aad Vad Fcad Al2O3 CaO 含量 7.60 3.73 75.00 2.18 2.29 注: Aad表示灰分;Vad表示挥发分;Fcad表示固定碳。1.2 实验程序
镍铁渣、兰炭粉、无水CaCl2充分混合后用50 kN的压力压制成φ20 mm×10 mm的圆柱体样品,样品称重后装入刚玉坩埚,盛样的坩埚送入箱式电阻炉,以15 ℃/min将炉温升至实验所设定温度并保温一定的时间,保温结束后,坩埚及样品随炉冷却至室温,冷却后样品称重、检测其中的镁含量,计算镁的挥发率,用XRD检测主要物相。
镁挥发率的计算方法见式(1):
(1) 式(1)中:
镁挥发率的数值,单位%;m1为加热前样品质量的数值,单位g;s1 加热前样品镁含量的数值,单位%;m2 加热后样品质量的数值,单位g;s2 加热后样品镁含量的数值,单位%。 2 结果与讨论
2.1 镍铁渣中镁的氯化挥发热力学及氯化过程渣相转变特征
2.1.1 镍铁渣中镁的氯化挥发热力学
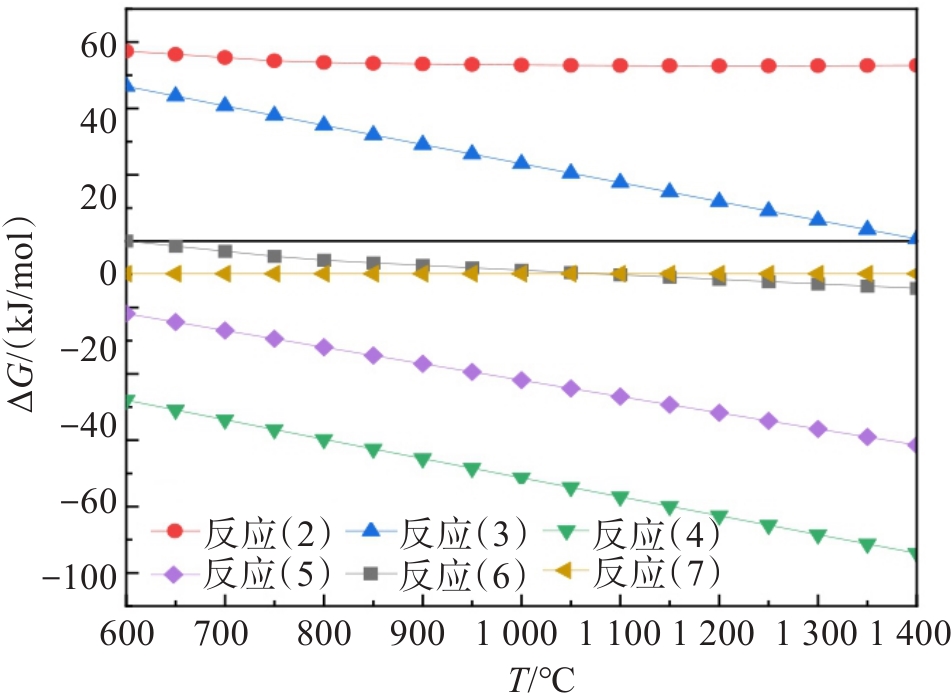
CaCl2氯化镍铁渣中的MgO过程中可能发生的反应见反应式(2)—式(7)[15, 21-22, 26-29],以HSC Chemistry 6.0软件的Reaction Equations模块计算各个可能反应在600~1 400 ℃的吉布斯自由能,各物质的热力学数据使用HSC Chemistry 6.0软件的数据库,各反应吉布斯自由能与温度之间的关系见图2。
2CaCl2+O2(g)=2CaO+2Cl2(g) (2) 2MgO+2Cl2(g)=2MgCl2(g)+O2(g) (3) 2MgO+2Cl2+C=2MgCl2(g)+CO2(g) (4) MgO+Cl2(g)+C=MgCl2(g)+CO(g) (5) 2CaCl2+O2(g)+2Al2O3+4SiO2=2CaO·Al2O3·2SiO2+2Cl2(g) (6) CaO+Mg2SiO4=MgO+CaMgSiO4 (7) 在计算的温度范围内,CaCl2不能分解为CaO和Cl2(见式(2));渣中酸性氧化物组分可以促进CaCl2分解生成Cl2[29],镍铁渣中含有Al2O3和SiO2,Al2O3和SiO2在600 ℃以上可以使CaCl2分解释放出Cl2(见式(6)); Cl2无法直接将MgO氯化(见式(3)),有碳参与反应时才能使Cl2将MgO氯化为MgCl2(见式(4)、式(5)),加碳氯化反应过程中碳更倾向于生成CO2(见式(4))。理论上以上反应均可在600 ℃以上进行,并且随着温度升高,氯化反应更易进行。
碳共存条件下CaCl2氯化渣中镁的过程为:
1)CaCl2在Al2O3、SiO2和O2作用下分解产出Cl2和2CaO·Al2O3·2SiO2。
2)Cl2与渣中MgO及配入的碳反应生成MgCl2气体。
3)由CaCl2分解生成的CaO逐渐增多,CaO可以与物料中的Mg2SiO4反应生成CaMgSiO4并游离出MgO(式(7)),游离出的MgO继续与CaCl2进行氯化反应。
2.1.2 氯化过程渣相转变特征
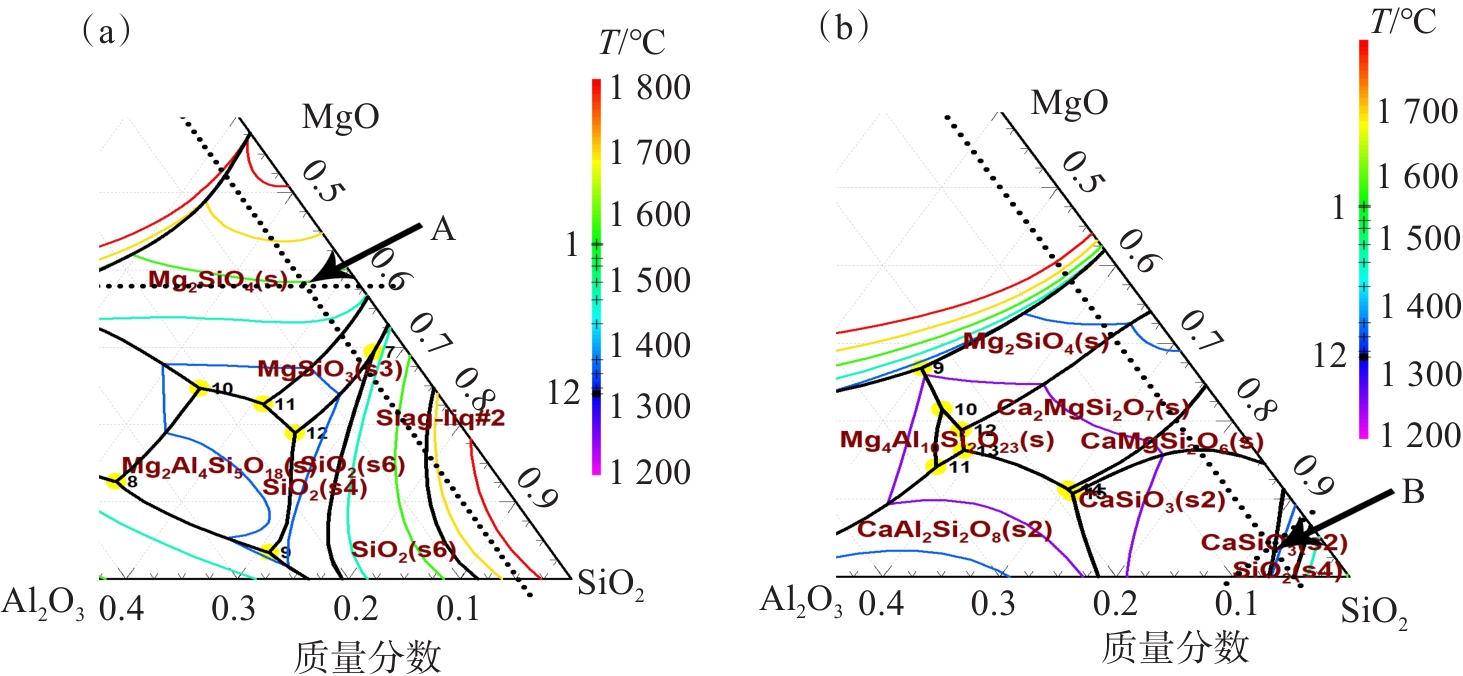
镍铁渣用CaCl2氯化渣中镁的过程中,CaCl2分解生成CaO,CaO含量增加,MgO含量降低,渣的物相、熔化性温度等特性会随之改变。采用Factsage软件分别计算了CaO含量在5.74%和31.11%时MgO-SiO2-Al2O3-CaO系的氯化渣相图,计算结果见图3。图3(a)所示为CaO含量为5.74%时MgO-SiO2-Al2O3-CaO系的渣相图(富SiO2角),图3(b)所示为CaO含量为31.11%时MgO-SiO2-Al2O3-CaO系的渣相图(富SiO2角)。
在氯化反应初期,渣相中主要成分为镍铁渣,根据镍铁渣中Al2O3及MgO的含量确定渣的物系点为图3(a)中的A点,A点区域主要物相为镁橄榄石,根据等温线,镁橄榄石的熔化性温度在1 400 ℃左右。随着氯化过程的进行,渣中MgO含量降低,CaO含量升高,以MgO含量为10%,Al2O3含量为5%确定渣的物系点为图3(b)中的B点,B点物相主要为CaSiO3,由该区域等温线判断,该区域的熔化性温度在1 300 ℃左右。由热力学计算结果可得,温度越高时,氯化反应越容易进行,因此在渣相熔化性温度由1 400 ℃向1 300 ℃转变过程中能够使氯化反应进行得较充分。可以预测,在热渣中进行氯化,待MgO充分挥发后,渣可能具有流动性[30]。
2.2 镍铁渣中镁的氯化研究
2.2.1 加热温度对镁挥发率的影响
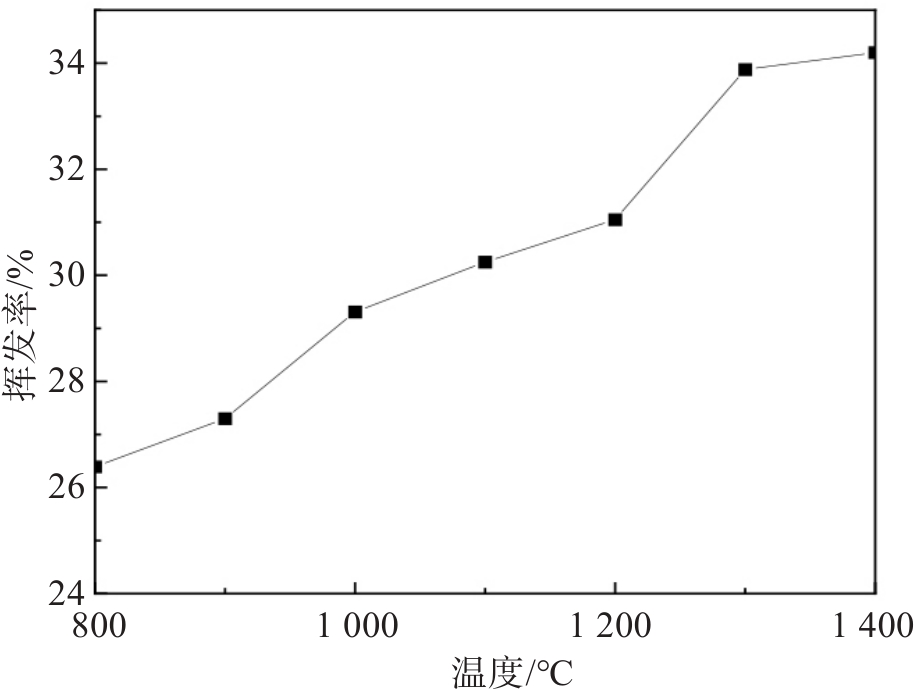
在n(CaCl2)/n(Mg)=1,n(C)/n(Mg)=1时,将混合物料压块后升高至不同温度并保温30 min。温度对镁挥发率的影响见图4。由图4可知,镁的挥发率随温度的升高而逐渐增大,在1 200~1 300 ℃,镁的挥发率增幅较大。在1 300 ℃时,镁的挥发率可以达到33.88%,在1 400 ℃时镁的挥发率为34.20%,在1 300~1 400 ℃时,镁的挥发率增幅较小,趋于稳定。
CaCl2的熔点为782 ℃[31],在800~1 200 ℃之间CaCl2为液态,镍铁渣为固态,两者之间发生液-固反应。根据反应式(6),在800~1 200 ℃之间,渣中的酸性氧化物如Al2O3和SiO2的化合物能够与CaCl2反应而释放出Cl2,根据反应式(4)及反应式(5),Cl2与碳共同与渣中的MgO发生反应而生成MgCl2并挥发;当加热温度在1 200~1 300 ℃时,混合物料中既有液态CaCl2,也有镍铁渣熔体,参与反应的物料量增加,使氯化速度提高,镁的挥发率增幅较大。当温度达到1 400 ℃时,固体物料大部分转变为液态,尽管液态时反应的物料量增加,但液态物料也阻碍了O2向物料中的扩散,抑制了CaCl2分解产出Cl2的反应,因此在高温时镁挥发率增幅较小。
2.2.2 碳配入量对镁挥发率的影响
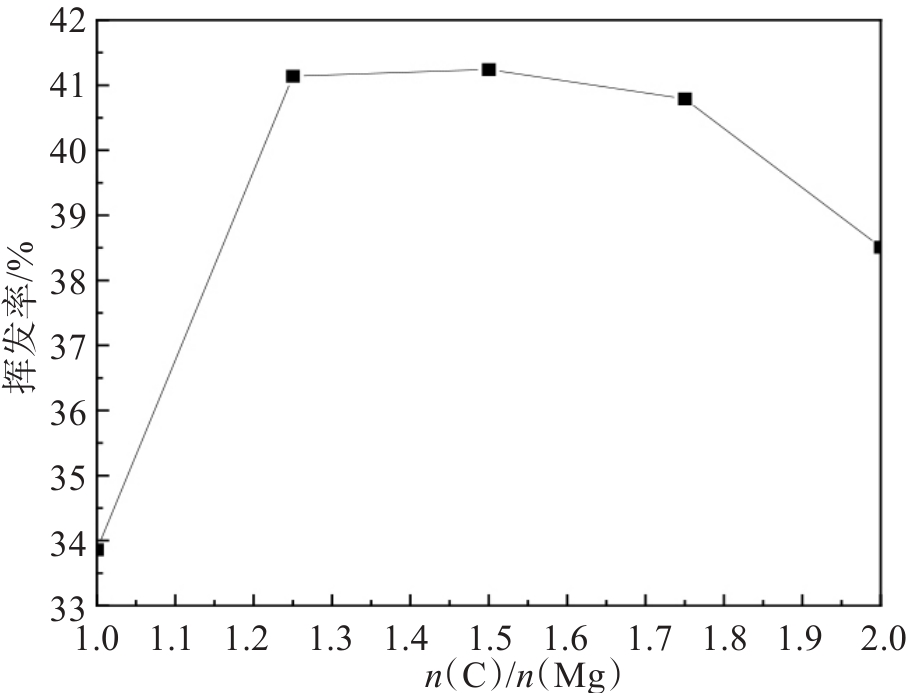
在加热温度为1 300 ℃,n(CaCl2)/n(Mg)=1,保温时间30 min时,选定不同的n(C)/n(Mg)。镁挥发率与配碳量的关系如图5所示。由图5可得,当n(C)/n(Mg)在 1.0~1.25之间时, 镁的挥发率增幅较大; 当n(C)/n(Mg)=1.25时,镁的挥发率为41.14%; 当n(C)/n(Mg)在1.25~1.5之间时,镁挥发率趋于稳定;当n(C)/n(Mg)大于1.5时,镁的挥发率有下降趋势。
随着氯化过程的进行,压块中的碳颗粒在逐渐消耗,混合物料中适当比例的碳可增加压块的空隙,减小了MgCl2气体向团块外部扩散的阻力,提高MgCl2的扩散挥发速度;CaCl2在有O2时才能分解产出Cl2(式(6)),当n(C)/n(Mg)大于1.25时,混合物料中的碳含量高,碳会与加热炉内的O2反应而使炉内O2含量降低,O2含量过低时,CaCl2分解放出Cl2的反应停止而无Cl2产出,则MgO的氯化反应随之停止,使镁的挥发率降低。
2.2.3 CaCl2配入量对镁挥发率的影响
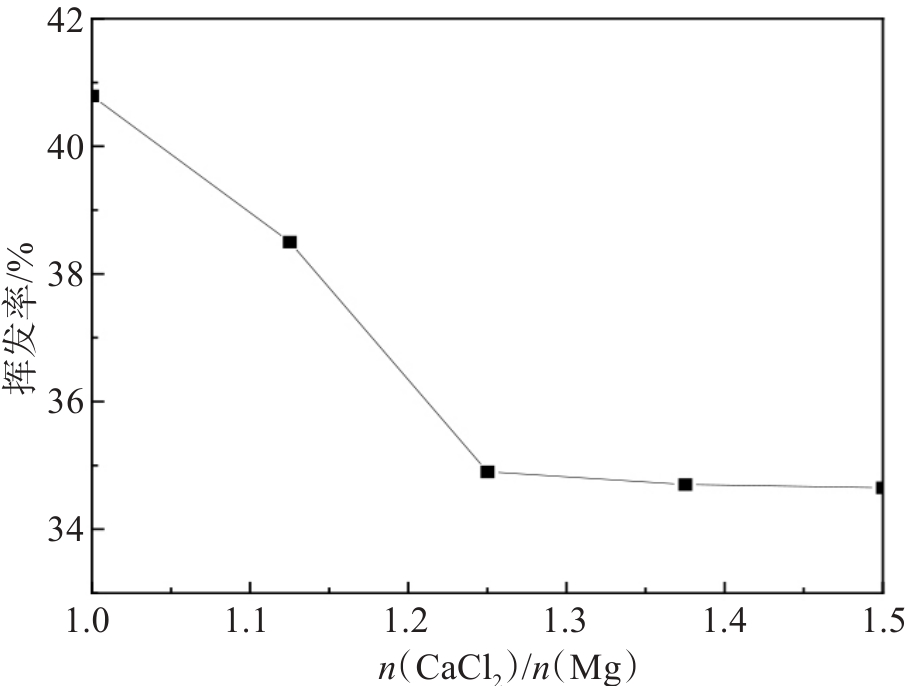
n(C)/n(Mg)=1.25,加热温度1 300 ℃,保温时间30 min,根据设定的n(CaCl2)/n(Mg)制样并进行镁的氯化挥发。镁挥发率与CaCl2配入量之间的关系见图6。由图6可得,当n(CaCl2)/n(Mg)=1时,镁的挥发率为40.79%,随着CaCl2配入量的增加,镁的挥发率降低;当n(CaCl2)/n(Mg)≥1.25时,镁的挥发率降到34.90%,并基本保持稳定。
CaCl2熔点较低,在高温时CaCl2转变为液态,液态CaCl2会堵塞压块中的空隙,阻碍O2扩散进入团块内部,使CaCl2分解为Cl2的反应无法进行,无法实现氯化。
2.2.4 氯化时间对镁挥发率的影响
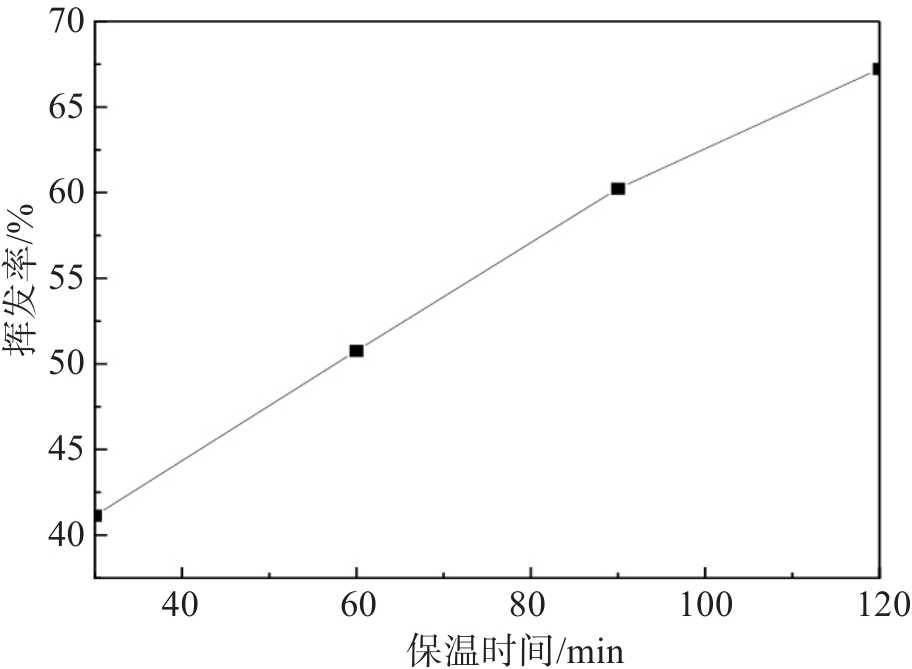
当n(C)/n(Mg)=1.25,n(CaCl2)/n(Mg)=1时,将混合物料压块加热至1 300 ℃后保温不同的时间。镁的挥发率与保温时间的关系见图7。由图7可得,镁的挥发率随保温时间延长逐渐升高,当保温时间为120 min时,挥发率达到最大值为67.22%,渣中MgO含量降低至8.21%。随着保温时间的延长,O2能充分向压块表面及内部扩散,使CaCl2较充分地分解出Cl2,同时延长保温时间,不仅延长了CaCl2的分解时间,产出更多Cl2,而且增加了物料间的接触时间,从而使镁的挥发率提高。
2.2.5 镍铁渣氯化后的渣成分及物相
在n(C)/n(Mg)=1.25,n(CaCl2)/n(Mg)=1时,分别对1 200 ℃和1 300 ℃保温120 min氯化后获得的渣进行物相检测,检测结果见图8,1 300 ℃氯化后的渣中主要成分检测结果见表3。氯化过程是MgO降低和CaO增加的过程,由图3(a)和图3(b)可得,氯化过程使渣的熔化性温度逐渐降低,以表3中渣的主要成分与图3(b)对照可得,理论上经氯化后渣中主要物相为CaSiO3,渣的初晶温度在逐渐降低,随着氯化反应的进行,CaO在渣中的含量增加,CaO含量增加可以降低渣的黏度[32],渣黏度降低,将有助于氯化反应过程的传质。
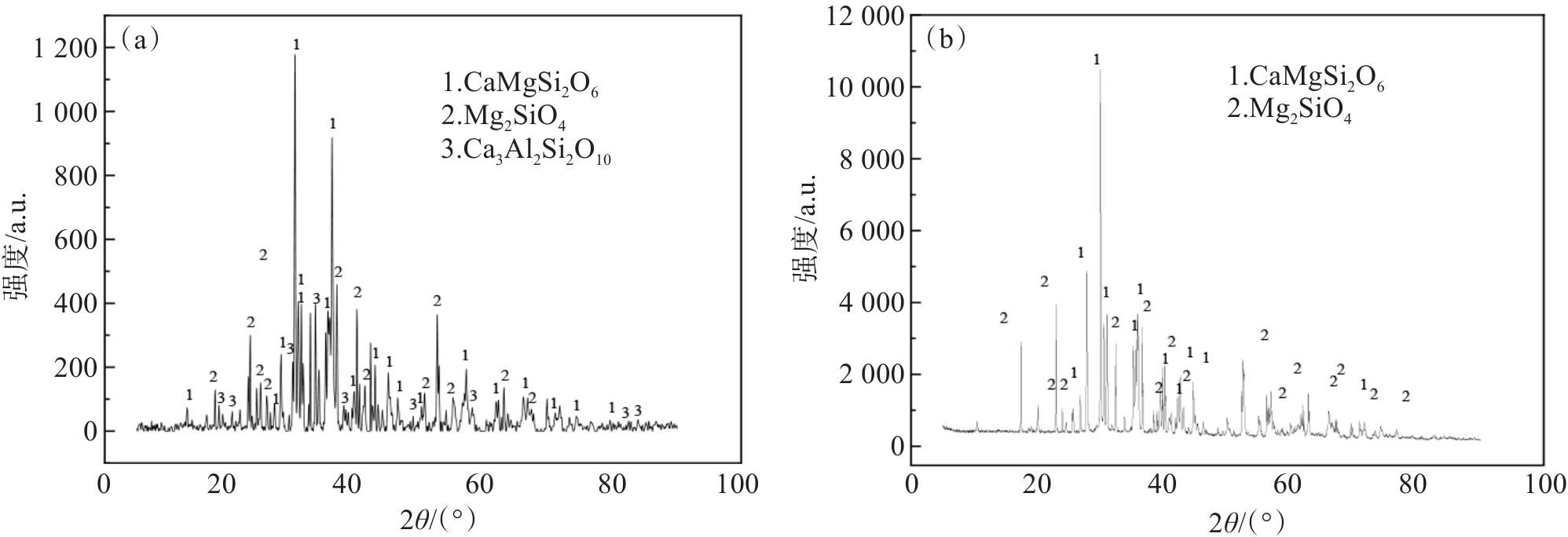
![]() 图 8 不同温度下镍铁渣氯化除镁后渣中的主要物相:(a) 1 200 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 min; (b) 1 300 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 minFigure 8. Main phases in the ferronickel slag after magnesium removal by chlorination at different temperatures:(a) 1 200 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 min; (b) 1 300 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 min表 3 氯化后渣中主要成分Table 3. Main components in the slag after chlorination
图 8 不同温度下镍铁渣氯化除镁后渣中的主要物相:(a) 1 200 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 min; (b) 1 300 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 minFigure 8. Main phases in the ferronickel slag after magnesium removal by chlorination at different temperatures:(a) 1 200 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 min; (b) 1 300 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 min表 3 氯化后渣中主要成分Table 3. Main components in the slag after chlorination成分 Fe2O3 SiO2 Al2O3 MgO CaO 含量 2.83 45.15 5.14 8.21 34.14 由图8(a)可得,1 200 ℃氯化后渣中的主要物相为CaMgSi2O6,Mg2SiO4和Ca3Al2Si2O10,与镍铁渣中主要物相(图1)相比,在1 200 ℃氯化后,渣中出现了CaMgSi2O6和Ca3Al2Si2O10,说明CaO已进入镍铁渣相并形成了新相。氯化过程CaCl2转变为CaO,CaO可促进镁橄榄石的分解,从而产生游离MgO[33],CaO的增加,促进了镍铁渣中镁橄榄石的分解,生成了新的CaMgSi2O6和Ca3Al2Si2O10相。1 300 ℃时,氯化渣中主要物相为CaMgSi2O6和Mg2SiO4,与1 200 ℃时氯化渣中的物相相比,Ca3Al2Si2O10相消失。随着加热温度升高,Ca3Al2Si2O10相可能转变为玻璃体而导致其衍射峰消失。
3 结 论
以CaCl2为氯化剂,在碳共存的条件下研究了高镁镍铁渣中镁的氯化挥发,获得了以下结论:
1)在n(C)/n(Mg)=1.25、n(CaCl2)/n(Mg)=1、1 300 ℃保温120 min条件下,镍铁渣中镁的挥发率达到67.22%,氯化后渣中MgO含量为8.21%。
2)镍铁渣中镁的氯化过程为:高温条件下镍铁渣中的酸性氧化物促进CaCl2分解出Cl2和CaO,CaO可促进Mg2SiO4分解生成游离MgO,Cl2与MgO反应生成MgCl2和O2,碳与O2反应降低了O2分压,促进了氯化反应的进行。
3)氯化渣中的主要物相为CaMgSi2O6和Mg2SiO4。随着氯化过程的进行,混合物料中的MgO含量逐渐降低,CaO含量增加,渣中主要物相由Mg2SiO4相转变为CaMgSi2O6相,渣的初晶温度逐渐降低。
4)氯化过程的气氛中需要保持一定量的氧含量,气氛中氧含量过低将会抑制氯化反应的进行。
王庆龙 -
图 8 不同温度下镍铁渣氯化除镁后渣中的主要物相:(a) 1 200 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 min; (b) 1 300 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 min
Fig 8. Main phases in the ferronickel slag after magnesium removal by chlorination at different temperatures:(a) 1 200 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 min; (b) 1 300 ℃, n(C)/n(Mg)=1.25, n(CaCl2)/n(Mg)=1, 120 min
表 1 镍铁渣主要成分
Table 1 Main components of ferronickel slag
成分 Fe2O3 SiO2 Al2O3 MgO CaO 含量 3.26 51.92 5.63 26.31 1.82 表 2 兰炭主要成分
Table 2 Main components of semi-coke
成分 Aad Vad Fcad Al2O3 CaO 含量 7.60 3.73 75.00 2.18 2.29 注: Aad表示灰分;Vad表示挥发分;Fcad表示固定碳。表 3 氯化后渣中主要成分
Table 3 Main components in the slag after chlorination
成分 Fe2O3 SiO2 Al2O3 MgO CaO 含量 2.83 45.15 5.14 8.21 34.14 -
[1] HAN F H, ZHANG H B, LI Y C, et al. Recycling and comprehensive utilization of ferronickel slag in concrete[J]. Journal of Cleaner Production, 2023, 414: 137633.
[2] KURNIATI E O, PEDERSON F, KIM H J. Application of steel slags, ferronickel slags, and copper mining waste as construction materials: a review[J]. Resources, Conservation and Recycling, 2023, 198: 107175.
[3] NURUZZAMAN M, AHMAD T, SARKER P K, et al. Rheological behaviour, hydration, and microstructure of self-compacting concrete incorporating ground ferronickel slag as partial cement replacement[J]. Journal of Building Engineering, 2023, 68: 106127.
[4] 熊远亮, 朱玉, 李保亮, 等. 镍铁渣砂对泡沫混凝土孔结构及收缩开裂性能的影响[J]. 硅酸盐通报, 2022, 41(8): 2792-2799. [5] 刘家辉, 宁志强, 谢宏伟, 等. 氧化镁的制备方法及发展趋势综述[J]. 有色金属科学与工程, 2021, 12(3): 12-19. [6] ZHU D Q, PAN L T, GUO Z Q, et al. Utilization of limonitic nickel laterite to produce ferronickel concentrate by the selective reduction-magnetic separation process[J]. Advanced Powder Technology, 2019, 30(2): 451-460.
[7] ZHANG X, GU F Q, PENG Z W, et al. Recovering magnesium from ferronickel slag by vacuum reduction: thermodynamic analysis and experimental verification[J]. ACS Omega, 2019, 4(14): 16062-16067.
[8] 李凤善, 马艺璇, 黄忠源, 等. 镍铁渣中硅铁镁元素提取热力学计算[J]. 冶金设备, 2021(增刊1): 27-30. [9] LI R, WANG L P, YANG B, et al. Recovery of AZ91D magnesium alloy waste by vacuum gasification-Directed condensation[J]. Vacuum, 2023, 212: 112048.
[10] GAO F, HUANG Z C, LI H, et al. Recovery of magnesium from ferronickel slag to prepare hydrated magnesium sulfate by hydrometallurgy method[J]. Journal of Cleaner Production, 2021, 303: 127049.
[11] 黄治成, 高锋, 李新生, 等. 硫酸法常压浸出镍铁渣中镁的正交试验及动力学分析[J]. 有色金属(冶炼部分), 2020(1): 18-21. [12] 陈金龙, 代龙果, 李玉虎, 等. 碳化沉淀法从中和渣浸出除杂液中分离回收锌和镁[J]. 有色金属科学与工程, 2022, 13(5): 1-7. [13] PRASETYO A B, DARMAWANSYAH R, MAYANGSARI W, et al. Reverse leaching of magnesium from ferronickel slag using alkali solvent NaOH[J]. Eastern-European Journal of Enterprise Technologies, 2020, 12(103): 6-14.
[14] 李大江, 郭持皓, 袁朝新, 等. 氰化尾渣氯化焙烧提金工艺及经济性研究[J]. 中国资源综合利用, 2018, 36(8): 45-46, 49. [15] 刘慧南, 胡杨甲, 吴桂叶, 等. 氯化挥发法从含有价金属硫铁矿精矿中回收金银[J]. 有色金属(冶炼部分), 2019(12): 44-48, 91. [16] 孙彦文, 袁朝新, 郭持皓, 等. 氰化尾渣熔融氯化提金银试验[J]. 矿冶, 2019, 28(6): 41-44. [17] 张树科, 曲邦定. 含金物料高温氯化挥发提金试验研究[J]. 中国资源综合利用, 2020, 38(2): 8-10. [18] 李保亮, 王月华, 潘东, 等. 电弧炉镍铁渣砂和镍铁渣粉的组成特性与适用性分析[J]. 材料导报, 2019, 33(22): 3752-3756. [19] BAI S J, WEN S M, CHEN Y, et al. Response surface methodology for optimization of the chloridizing roasting process for a high copper pyrite cinder[J]. Advanced Materials Research, 2012, 524/525/526/527: 1070-1077.
[20] XUE K, JIAO F, LI W, et al. Using magnesium chloride to volatilize impurity metals from waste magnesia-chromium refractories[J]. JOM, 2022, 74(4): 1350-1359.
[21] 胡若翀, 廖春发, 张忠堂, 等. 从铜阳极泥中短流程分离富集稀贵元素新工艺研究[J]. 江西冶金, 2023, 43(4): 306-313. [22] 肖金田. 提高氯化炉产能的一种新还原剂—氧化镁球团氯化用褐煤焦作还原剂的研究[J]. 轻金属, 1990(11): 41-45. [23] CHUBUKOV B A, ROWE S C, PALUMBO A W, et al. Investigation of continuous carbothermal reduction of magnesia by magnesium vapor condensation onto a moving bed of solid particles[J]. Powder Technology, 2020, 365: 2-11.
[24] 郑权. 镁电解质挥发特性研究[J]. 有色金属科学与工程, 2015, 6(6): 47-51. [25] 赵景富. 红土镍矿生产高品位镍铁试验研究[J]. 铁合金, 2022, 53(3): 21-24. [26] 李磊, 张仁杰, 胡建杭. 用氯化焙烧法脱除炼铜炉渣中的铜[J]. 材料研究学报, 2016, 30(2): 99-106. [27] 张仁杰, 李磊, 韩文朝. 氯化焙烧法回收铜渣中铜的热力学研究[J]. 工业加热, 2014, 43(1): 4-9. [28] 伏晓丹, 张海宝, 陈燕杰, 等. 某低品位氧化铜矿堆浸液萃取铜的试验研究[J]. 江西冶金, 2024, 44(1): 43-47. [29] 张倍恺, 郭学益, 王亲猛, 等. 氯化焙烧铜熔炼渣回收铅工艺及动力学研究[J]. 矿冶工程, 2022, 42(1): 72-76. [30] 王震, 沈峰满, 刘春城, 等. 高铝高炉渣系的熔化特性[J]. 钢铁, 2022, 57(2): 36-45. [31] 梁振凯, 雷雪飞, 孙应龙, 等. 氯化钙焙烧法提取粉煤灰中的氧化铝[J]. 中国环境科学, 2013, 33(9): 1601-1606. [32] 张思奇, 于阔沛, 倪文, 等. 铁合金热熔渣成分调质对矿棉性能的影响[J]. 铁合金, 2020, 51(5): 38-45. [33] HAN J B, FU D X, GUO J H, et al. Volatilization and condensation behavior of magnesium vapor during magnesium production via a silicothermic process with magnesite[J]. Vacuum, 2021, 189: 110227.



 下载:
下载: