Effect of precursor pretreatment on the electrochemistry of lithium-rich manganese oxides
-
摘要: 实验通过小规模共沉淀和固相反应成功合成了无钴富锂锰基前驱体Ni0.3Mn0.7(OH)2,将前驱体不进行和进行机械粉碎,分别得到2种不同粒径的Ni0.3Mn0.7(OH)2(D50=1.626 µm和0.710 µm)前驱体。不同粒径大小的前驱体与LiOH以1∶1.55的摩尔比混合,经过高温烧结,合成2种颗粒大小的富锂锰基正极材料Li1.2Ni0.24Mn0.56O2 (D50=1.667 µm和1.148 µm)。实验结果表明,颗粒尺寸影响其物理化学性质和电化学性能。Li1.2Ni0.24Mn0.56O2 (D50=1.148 µm)正极材料具有较小颗粒尺寸,显示出优异的电化学性能(在0.5 C下循环100次后,容量为190.7 mAh/g,循环保持率高达91.2%)。研究揭示了一种简易方法改变颗粒大小,并证明了粒径对电化学的重要性。Abstract: In this experiment, the cobalt-free lithium-rich manganese precursor Ni0.3Mn0.7(OH)2 was successfully synthesized by small-scale co-precipitation and solid-phase reaction, and the precursor was mechanically crushed with or without the precursor to obtain two different particle sizes of Ni0.3Mn0.7(OH)2 (D50=1.626 µm and 0.710 µm) precursors. The precursors with different particle sizes were mixed with LiOH in a molar ratio of 1:1.55 and sintered at high temperature to synthesize two Li Mn-rich cathode materials with different particle sizes, Li1.2Ni0.24Mn0.56O2 (D50=1.667 µm and 1.148 µm). The experimental results show that the particle size also affects its physicochemical properties and electrochemical performance. Li1.2Ni0.24Mn0.56O2 (D50=1.148 µm) cathode material with smaller particle size shows excellent electrochemical performance (capacity of 190.7 mAh/g after 100 cycles at 0.5 C and cycle retention rate of 91.2%). Our study reveals an easy way to change the particle size and demonstrates the importance of particle size for electrochemistry.
-
微合金技术是20世纪钢铁工业领域最突出的成就之一[1], 将Ti、Nb、V等微合金元素加入普通碳素钢中, 可显著提升钢材的强度、韧性等性能, 并广泛应用于国民经济及国防工业的各个领域[2].近年来, 微合金钢性能的提升已逐步成为反映国家钢铁工业水平的重要标志.历经日本[3]、韩国[4]和中国[5]等钢铁大国数十年来的发展, 微合金钢强化机理研究已逐步由细晶强化转变为析出强化.
析出强化是通过钢中弥散分布的细小析出相(纳米碳化物), 与位错发生交互作用而提高钢强度的强化方式[6].根据位错与析出相交互作用的差异, 析出强化表现出2种不同的强化机制:一是析出相尺寸较小, 位错运动切割质点造成共格应变的切割机制[7-8]; 二是析出相尺寸较大, 位错运动绕过质点造成共格关系完全破坏的绕过机制[9].近年来, 日本JFE钢铁公司采用0.04 %C-1.5 %Mn-0.09 %Ti-0.2 %Mo的成分体系, 利用析出强化方式成功开发出780 MPa级汽车用板带钢[10], 目前已发展至1 180 MPa级[11].
尽管已针对微合金钢中纳米碳化物的析出规律和强化机理开展了大量研究工作[12-16], 但纳米碳化物的定量分析研究仍有待进一步发展.随着纳米表征技术的发展, 钢中纳米碳化物的分析手段也在不断进步, 分辨率达0.2 nm的透射电子显微镜可清晰观测钢中纳米碳化物.归纳而言, 目前, 透射电子显微镜的试样制备有以下3种方法:第1, 钢样直接减薄观测, 包括离子减薄和双喷减薄[12, 17], 论文采用双喷减薄; 第2, 萃取复型纳米碳化物观测[15, 18]; 第3, 无损电解提取纳米碳化物观测[2], 并结合化学相分析[19]及X射线小角散射[20]获得纳米碳化物的物相组成及粒度分布特征.尽管纳米碳化物分析方法已逐步明确, 但尚未对其进行深入对比.因此, 文中以Ti微合金钢为研究对象, 分别采用上述3种分析方法考察纳米碳化物并进行对比, 探讨不同分析方法的适用范围.
1 材料及方法
实验用Ti微合金钢的化学成分如表 1所列, 将其置于1 250 ℃电阻炉中保温3 h, 然后, 在Ф450 mm辊式热轧机组和超快速冷却装置上将钢坯厚度由100 mm轧制至12 mm, 轧制工艺参数如表 2所列.
表 1 Ti微合金钢的化学成分/(质量分数, %)Table 1. Chemical composition of Ti microalloyed steel /(mass fraction, %)元素名称 C Mn Si P S Nb Ti A1 N 0 成分 0.15 0.98 0.28 0.015 0.005 0 0.08 0.02 (4.0~5.0)×10-5 (4.0~5.0)×l0-5 表 2 轧制工艺参数Table 2. Rolling process parameters粗轧温度/℃ 精轧温度/℃ 水冷速度/(℃·s-1) 轧制规格/mm 1 050 860 40 12 Ti微合金钢轧制完成后, 采用以下3种方法处理.第1, 直接减薄, 在钢样中心处切取薄膜样品并机械减薄至50 μm, 然后采用双喷减薄仪进行减薄, 并使用透射电子显微镜对纳米碳化物进行观察.第2, 萃取复型, 钢样打磨抛光后在5 %硝酸酒精溶液中深腐蚀, 在腐蚀好的金相样上蒸发沉积一层较厚碳膜后, 将其再次放入硝酸酒精溶液中进行二次侵蚀以分离复型样品, 将复型样品置于铜网上后使用透射电子显微镜对纳米碳化物进行观察.第3, 无损电解, 采用无损电解提取技术将纳米碳化物从组织中电解出来, 经选择性分离可得到MC和M3C型纳米碳化物, 进一步使用化学相分析(包括XRD, 相类型鉴定及结构分析)、X射线小角散射及透射电子显微镜等检测方法, 获得纳米碳化物的物相组成、粒度分布及形貌特征.
2 结果及讨论
2.1 直接减薄
直接减薄样品中纳米碳化物的分布情况如图 1所示.该实验条件下, Ti微合金钢存在板条状组织, 且大量纳米碳化物钉扎于高密度的位错线和位错胞附近, 强化钢铁韧性.此外, 纳米碳化物亦可在晶界附近聚集(如图 1(c)), 通过明、暗场像对比可知, 该视场下主要为60~100 nm纳米碳化物.晶界附近聚集形成纳米碳化物的主要原因有以下两方面:其一, 晶体形成中, 晶体在结晶凝固的过程中不断将高熔点的碳化物推向晶界, 并最终聚集于最后结晶的晶界附近; 其二, 晶体形成后, 能量较高的晶界区域容易形核, 从而促进碳化物析出.
为明确Ti微合金钢中纳米碳化物的化学成分, 进一步对图 1中纳米碳化物进行EDS能谱分析, 典型EDS能谱结果如图 2所示.能谱结果表明:直接减薄样品中所观察到的纳米碳化物主要为M3C型纳米碳化物, 且在该视场下并未发现MC型纳米碳化物.
2.2 萃取复型
由于微合金钢基体的干扰, 使得采用上述直接减薄样品时, 难以观测MC型纳米析出物.因此, 将纳米碳化物与微合金钢基体分离, 可有效解决上述问题.
MC型纳米碳化物的透射电镜明场像、电子衍射谱及EDS能谱如图 3所示. 图 3中MC型纳米碳化物尺寸约为100 nm, 且呈现四边形结构.钢中MC型纳米碳化物形貌大体呈现四边形的原因为:当奥氏体开始析出MC时, 在界面能的作用下, 析出物基本保持球形, 但随着析出物不断长大, 界面能逐渐失去主导地位, 而界面台阶处则成为新扩散来的原子最佳附着反应位置, 进而使得析出物逐步转变为四边形.
此外, 萃取复型样品观察到了针状M3C型纳米碳化物, 其透射电镜明场像、电子衍射谱及EDS能谱如图 4所示.但是, 由于碳膜强度及M3C型纳米碳化物与微合金钢基体的结合强度等问题, 萃取复型样品并未体现出类似于直接减薄样品中M3C型纳米碳化物的数量优势.同时, 由于已将纳米碳化物与基体分离, 故无法观测纳米碳化物在基体中的析出位置及与基体晶格之间的原子排列取向关系.
2.3 无损电解
为提高对纳米碳化物的观察效果, 在无损电解提取纳米碳化物后, 对其进行选择性分离, 将MC及M3C型碳化物分离开来进行透射电子显微镜表征、化学相分析及X射线小角散射.
1) 形貌特征. MC型纳米碳化物的透射电镜明场像、电子衍射谱及EDS能谱如图 5所示.从图 5中可观察到直径可达180 nm的单颗粒大尺寸MC析出物, 与萃取复型样品类似, 其形状亦基本呈四边形结构.二者对比可说明, 萃取复型和无损电解法不会影响纳米碳化物形貌特征.
相比于萃取复型方法, 通过无损电解方法可观察到针状和片状2种形态的M3C型析出物.针状M3C型纳米碳化物的透射电镜明场像、电子衍射谱及EDS能谱如图 6所示.片状M3C型纳米碳化物的透射电镜明场像、电子衍射谱及EDS能谱如图 7所示.本质而言, 片状M3C型纳米碳化物旋转90 °观察即可得到针状M3C型纳米碳化物, 故二者形态差异主要取决于观察角度.
2) 物相特征.由于无损电解方法提取的MC及M3C型纳米碳化物已被选择性分离, 故可分别针对二者开展化学相分析(包括XRD, 相类型鉴定及结构分析), 结果汇总于表 3. Ti微合金钢中纳米碳化物主要为M3C类型的(Fe0.986Mn0.014)3C, 其在钢中的质量分数达到了1.411 3 %; 而M (C, N) 类型的Ti (C0.672N0.328) 在钢中的质量分数仅为0.031 3 %.在文章采用的轧制工艺条件下, 前者是后者的45倍.正如前文所述, 由于MC型纳米碳化物的质量分数远低于M3C型纳米碳化物, 故通过直接减薄对其进行透射电镜分析需花费较大精力.因此, 为提高对MC型纳米碳化物的观察效果, 可采用萃取复型和无损电解等方法.
表 3 M3C及MC类纳米碳化物占钢的质量分数Table 3. Mass fraction of M3C and MC precipitates相类别 相结构 相占钢的质量分数/% 点阵常数/nm 晶系 MC Ti (C0.609Na391) 0.031 3 a0=0.429~0.430 面心立方 M3C (Fe0.986Mn0.014)3C 1.411 3 a0=0.448 3-0.451 0
b0=0.503 3~0.5080
c0=0.673 7-0.673 0正交 3) 粒度分布特征.采用X射线小角散射分别考察MC和M3C型纳米碳化物的粒度分布特征, 检测结果如图 8所示.由图 8可知, MC和M3C型纳米碳化物的平均粒度分别为102.30 nm和67.90 nm.整体而言, M3C型纳米碳化物粒度小于MC型纳米碳化物粒度.值得注意的是, 在文章采用的轧制工艺条件下, MC型纳米碳化物粒度分布呈现小尺寸颗粒和大尺寸颗粒较多, 而中间段尺寸颗粒较少的分布特征; M3C型纳米碳化物粒度分布呈现中间段尺寸颗粒较为集中的分布特征.
2.4 纳米碳化物分析方法的比较
综合上述分析可知, 直接减薄、萃取复型以及无损电解等方法均可用来分析微合金钢中纳米析出物, 但三者各有特色, 三者比较汇总于表 4.
表 4 微合金钢中纳米碳化物分析方法的比较Table 4. Comparison of different detection method of nano-carbide precipitates in microalloyed steel类别 直接减薄 萃取复型 无损电解 制样 简单 较为简单 复 与基体取向关系 保留 丢失 丢失 观察低质量分数纳米碳化物 不易 容易 容易 观察纳米碳化物区间 某一平面 平 某一尺寸体 可获纳米碳化物信息 形貌 形貌 物粒度分布 对于直接减薄而言, 其优势为保留了纳米碳化物与基体晶格之间的原子排列取向关系, 且制样过程简单; 但由于基体的干扰, 观察质量分数较低的纳米碳化物时需花费较大周期, 例如文中未观察到MC型纳米碳化物.此外, 其仅能观察某一平面的纳米碳化物特征, 结果具有一定偶然性.同时, 由于样品具有磁性, 存在损伤透射电子显微镜的可能.
对于萃取复型而言, 由于其消除了基体的干扰, 可清晰观察到质量分数较低的纳米碳化物, 并完全保留了纳米碳化物的形貌特征; 但却丢失了纳米碳化物与基体晶格之间的原子排列取向关系, 且同样仅能观察某一平面的纳米碳化物特征.同时, 相比于直接减薄, 萃取复型样品制备过程略微复杂.
对于无损电解而言, 与萃取复型类似, 其亦将纳米碳化物与基体分离, 但其分离的纳米碳化物并非属于某一平面, 而是属于某一尺寸立方体, 故更能完整代表纳米碳化物的形貌特征, 例如文中观察到了呈针状和片状的M3C型纳米碳化物.此外, 由于已将MC与M3C型纳米碳化物选择性分离, 故可分别对二者进行化学相分析和X射线小角散射, 进而明确二者的物相组成及粒度分布特征, 所获得实验结果更为全面.但是, 如同萃取复型, 该方法亦丢失了纳米碳化物与基体晶格之间的原子排列取向关系, 且制样过程远复杂于萃取复型.
综合而言, 3种微合金钢中纳米碳化物的分析方法各有优势, 在实际操作中, 应根据三者适用范围和检测需求进行合理选择, 以获得最佳检测效果.
3 结论
1) 将钢样直接减薄制备透射电子显微镜样品观察纳米碳化物, 制样过程简单, 可发现其大部分聚集于位错及晶界附近, 产生钉扎效应强化钢铁韧性; 但是, 由于基体的干扰, 在该平面视场范围内, 未发现质量分数较少的MC型纳米碳化物, 观察结果具有一定偶然性.
2) 萃取复型纳米碳化物进行观测, 制样过程较为简单, 并可较为容易观测到MC型纳米碳化物的形貌特征; 同时, 由于碳膜强度及碳化物与基体结合强度等因素, 萃取复型样品中M3C型纳米碳化物的数量优势并不明显; 此外, 与直接减薄样品类似, 对某一平面纳米碳化物观测具有一定偶然性.
3) 无损电解提取纳米碳化物, 并对其进行选择性分离可分别获得MC和M3C型纳米碳化物, 该方法制样过程极为复杂; 同时, 由于纳米碳化物取自某一尺寸立方体, 故纳米碳化物检测结果具有可重复性; 此外, 结合化学相分析和X射线小角散射, 可进一步获得纳米碳化物的物相组成和粒度分布特征, 检测结果全面.
赵中波 -
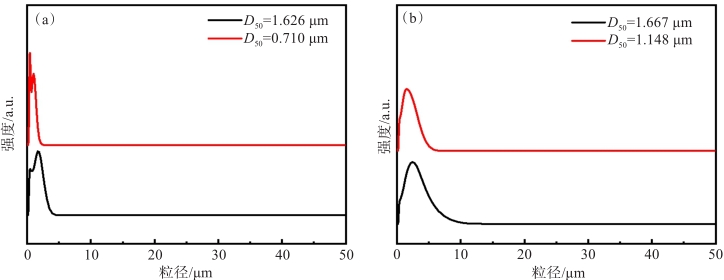
图 2 不同粒径的前驱体及其对应粒径的正极料样品的激光粒度图谱:(a) Ni0.3Mn0.7(OH)2 (D50=1.626 µm)样品;(b) Li1.2Ni0.24Mn0.56O2 (D50= 1.148 µm)样品
Fig 2. Laser particle size mapping of precursors of different particle sizes and their corresponding size of cathode material samples:(a) Ni0.3Mn0.7(OH)2 (D50=1.626 µm);(b)Li1.2Ni0.24Mn0.56O2 (D50= 1.148 µm)
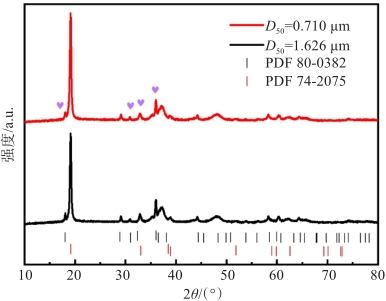
图 5 Li1.2Ni0.24Mn0.56O2(D50=1.667 和 1.148 µm)样品的XRD图谱和XRD精修图谱:(a) XRD图谱;(b) (003)峰的XRD放大图;(c) D50=1.667 µm样品的XRD精修图谱;(d) D50=1.148 µm样品的XRD精修图谱
Fig 5. XRD patterns and XRD refined patterns of Li1.2Ni0.24Mn0.56O2 (D50=1.667 µm and 1.148 µm) samples:(a)XRD pattern ; (b) the magniffed splitting pair peak of (003);(c) riveted reffnement results of D50=1.667 µm sample ; (d) riveted reffnement results of D50=1.148 µm sample
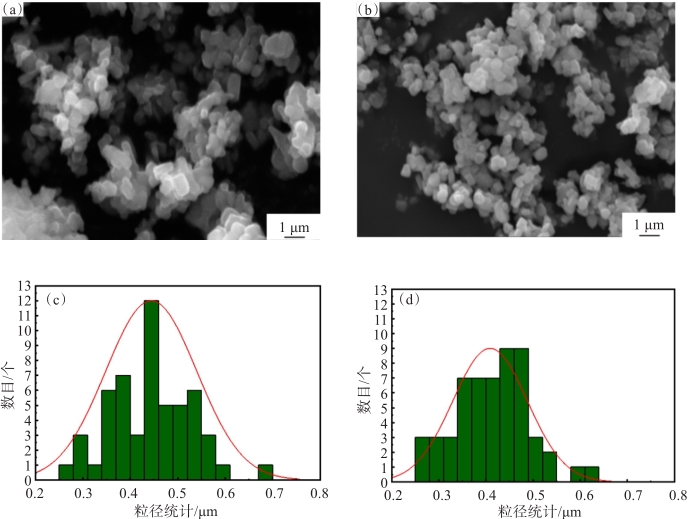
图 6 Li1.2Ni0.24Mn0.56O2 样品扫描电镜图像和粒度统计图:(a) D50=1.667 µm样品的SEM图谱;(b) D50=1.148 µm
样品的SEM图谱;(c) D50=1.667 µm样品的粒径统计图谱;(d) D50=1.148 µm样品的粒径统计图谱
Fig 6. SEM images and particle size statistics of Li1.2Ni0.24Mn0.56O2 samples: (a) SEM image of D50=1.667 µm sample ; (b) SEM image of D50=1.148 µm sample (c) particle size statistics of D50=1.667 µm sample;(d) particle size statistics of D50=1.148 µm sample
表 1 Li1.2Ni0.24Mn0.56O2(D50=1.667 µm和1.148 µm)样品R-3m和C2/m相晶格参数
Table 1 R-3m and C2/m phase lattice parameters of Li1.2Ni0.24Mn0.56O2 (D50=1.667 and 1.148 µm) samples
样品 a/Å c/Å c/a I(003)/I(104) Rwp/% Rp/% χ2 D50=1.667 µm 2.863 14.260 4.981 1.948 5.03 5.07 0.823 D50=1.148 µm 2.869 14.274 4.976 2.007 6.63 5.03 1.337 表 2 XPS图中的Mn2+/Mn3+和Ni2+/Ni3+相关峰面积数据
Table 2 Peak area data related to Mn2+/Mn3+ and Ni2+/Ni3+ in XPS plots
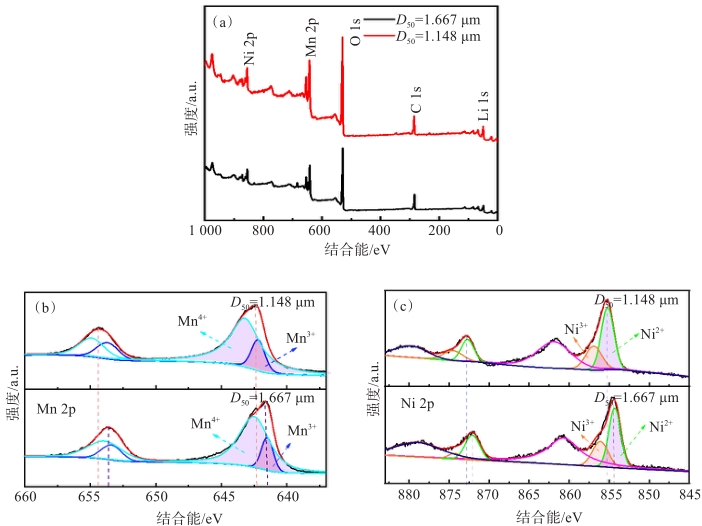
样品 Mn3+ Mn4+ Ni2+ Ni3+ D50=1.667 µm 17.4% 82.6% 66.9% 33.1% D50=1.148 µm 18.5% 81.5% 64.3% 35.7% 表 3 Li1.2Ni0.24Mn0.56O2(D50=1.667 µm和1.148 µm)的初始充放电数据
Table 3 Initial charge-discharge data of Li1.2Ni0.24Mn0.56O2 (D50 = 1.667 µm and 1.148 µm)
样品粒径 充电比容量/(mAh/g) 放电比容量/(mAh/g) 库仑效率/% D50=1.667 µm 268.7 213.9 79.6 D50=1.148 µm 306.8 246.7 80.4 -
[1] 胡伟, 钟盛文, 黄冰. 富锂锰基正极材料的改性及电化学性能研究[J]. 有色金属科学与工程, 2014, 5(4):32-36. [2] 段建峰, 钟盛文, 曾敏. 20 Ah富锂锰动力电池的性能研究[J]. 有色金属科学与工程, 2013, 4(2):37-40. [3] CHOU S L, WANG J Z, SUN J Z, et al. High capacity, safety, and enhanced cyclability of lithium metal battery using a V2O5 nanomaterial cathode and room temperature ionic liquid electrolyte[J]. Chemistry of Materials, 2008, 20(22): 7044-7051.
[4] 张盼盼, 黄惠, 何亚鹏, 等. 锂离子电池富锂锰正极材料的最新进展[J]. 材料工程, 2021, 49(3): 48-58. [5] DOGAN F, LONG B R, CROY J R, et al. Re-entrant lithium local environments and defect driven electrochemistry of Li-and Mn-rich Li-ion battery cathodes[J]. Journal of the American Chemical Society, 2015, 137(6): 2328-2335.
[6] BUMS J, OUYANG B, CHENG J L, et al. Equilibrium particle shape and surface chemistry of disordered Li-excess, Mn-rich Li-ion cathodes through first-principles modeling[J]. Chemistry of Materials, 2022, 34(16): 7210-7219.
[7] 刘志亮, 李小林, 雷超, 等. W 掺杂改性富锂锰层状正极材料[J]. 有色金属科学与工程, 2020, 11(6):57-63. [8] XIE X, LI H, CAO S, et al. Improving the cycling stability of Li-rich Mn-based cathodes through surface modification of VOPO4[J]. Energy & Fuels, 2021, 35(17): 14148-14156.
[9] WANG B, CUI J, LI Z J, et al. Surface F-doping for stable structure and high electrochemical performance of Li-rich Mn-based cathode materials[J]. Journal of Alloys and Compounds, 2022, 929: 167304.
[10] LIU J H, CHEN H Y, XIE J N, et al. Electrochemical performance studies of Li-rich cathode materials with different primary particle sizes[J]. Journal of Power Sources, 2014, 251: 208-214.
[11] HELBIG J, BEUSE T, SIOZIOS V, et al. Li/Mn-rich cathode materials with low-cobalt content and core-shell particledesign for high-energy lithium-ion batteries[J]. Journal of the Electrochemical Society, 2020, 167(6): 060519.
[12] LUO D, DING X K, HAO X D, et al. Ni/Mn and Al dual concentration-gradients to mitigate voltage decay and capacity fading of Li-rich layered cathodes[J]. ACS Energy Letters, 2021, 6(8): 2755-2764.
[13] ZHENG J, MYEONG S, CHO W, et al. Li-and Mn-rich cathode materials: challenges to commercialization[J]. Advanced Energy Materials, 2017, 7(6): 1601284.
[14] MA J, LI B, AN L, et al. A highly homogeneous nanocoating strategy for Li-rich Mn-based layered oxides based on chemical conversion[J]. Journal of Power Sources, 2015, 277: 393-402.
[15] 张宏生. 共沉淀控制结晶法制备富锂锰基锂离子电池正极材料的技术研究[D]. 杭州:浙江大学, 2014. [16] 丁晓凯. 无钴富锂锰基层状氧化物正极材料表面改性研究[D]. 广州:广东工业大学, 2022. [17] ARBIZZANI C, BALDUCCI A, MASTRAGOSTINO M, et al. Characterization and electrochemical performance of Li-rich manganese oxide spinel/poly (3, 4-ethylenedioxythiophene) as the positive electrode for lithium-ion batteries[J]. Journal of Electroanalytical Chemistry, 2003, 553: 125-133.
[18] 胡柳泉, 何杜, 廖达前, 等. 锂含量对富锂锰基正极材料 Li[LixNi0.13Co0.13Mn 0.54]O2 结构与电化学性能的影响[J]. 矿冶工程, 2015, 35(5): 113-116. [19] 班丽卿, 高敏, 庞国耀, 等. 富锂锰基 Li1.2[Co0.13Ni0.13Mn0.54]O2锂离子正极材料的磷改性研究[J]. 材料工程, 2020, 48(7): 103-110. [20] WANG Y Q, YANG Z Z, QIAN Y M, et al. New insights into improving rate performance of lithium‐rich cathode material[J]. Advanced Materials, 2015, 27(26): 3915-3920.
[21] 郭乾坤, 黄吉丽, 周苗苗, 等. 单晶 LiNi0.83Co0.1Mn0.07O2正极材料的合成及电化学性能[J]. 有色金属科学与工程, 2020, 11(4):23-28. [22] 段继东. 高性能层状富锂锰基正极材料的设计与电化学性能研究[D]. 绵阳: 西南科技大学, 2021. [23] HEKMATFAR M, KAZZAZI A, ESHETU G G, et al. Understanding the electrode/electrolyte interface layer on the Li-rich nickel manganese cobalt layered oxide cathode by XPS[J]. ACS Applied Materials & Interfaces, 2019, 11(46): 43166-43179.
[24] 李中, 洪建和, 何岗, 等. 富锂正极材料Li1.2Mn0.54Ni0.13Co0.13O2的FePO4包覆研究[J]. 无机材料学报, 2015, 30(2): 129-134. [25] 史晓岩. 富锂锰基体系电池产气及电化学性能研究[D]. 北京:北京有色金属研究总院, 2021. [26] NAVAK P K, ERICKSON E M, SCHIPPER F, et al. Review on challenges and recent advances in the electrochemical performance of high capacity Li-and Mn-rich cathode materials for Li‐ion batteries[J]. Advanced Energy Materials, 2018, 8(8): 1702397.
[27] HY S, FELIX F, RICK J, et al. Direct in situ observation of Li2O evolution on Li-rich high-capacity cathode material, Li[NixLi(1–2x)/3Mn(2-x)/3]O2 (0≤x≤0.5)[J]. Journal of the American Chemical Society, 2014, 136(3): 999-1007.
-
期刊类型引用(1)
1. 戎宇航,朱翔鹰,陈军修,吴长军,涂浩,王建华,苏旭平. Ti-Al-Fe-O熔体中氧化铝析出行为的研究. 有色金属科学与工程. 2024(01): 34-42 .  本站查看
本站查看
其他类型引用(1)



 下载:
下载: