Hydrothermal preparation of visible-light-activated photocatalyst Bi12TiO20 with different morphologies
-
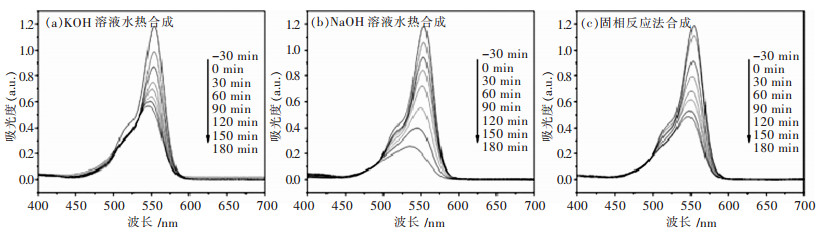
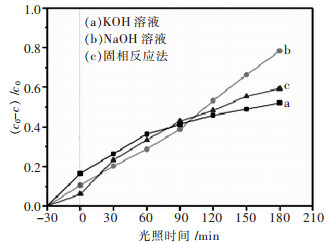
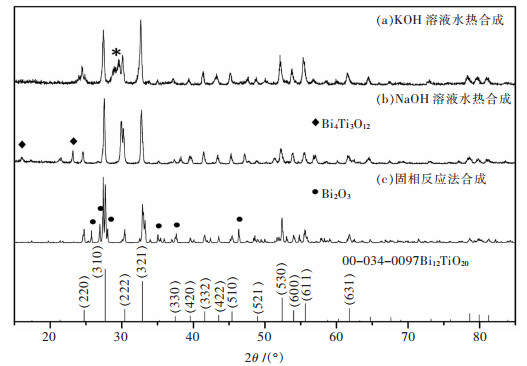
摘要: 以五水硝酸铋(Bi(NO3)3·5H2O)和钛酸四丁酯(Ti(OC4H9)4)为原料,采用水热法,在无表面活性剂的条件下成功制备出不同形貌的Bi12TiO20晶体.利用场发射扫描电镜和X射线衍射仪对产物的微观形貌和晶体结构进行了表征,结果表明,以KOH和NaOH为矿化剂可以分别得到纳米网状和片状的Bi12TiO20晶体,两者属于立方晶系.另外,以模拟太阳光为光源、罗丹明B为目标降解物测试了样品的光催化性能,结果显示,水热合成的Bi12TiO20晶体比固相反应法合成的样品具有更好的可见光光催化性能,其中,基于纳米片状结构Bi12TiO20晶体的罗丹明B溶液,光照180 min后的降解率可达78.2 %.Abstract: Bi12TiO20 crystals with different morphologies are prepared by a hydrothermal process with no surfactants using Bi (NO3)3·5H2O and Ti (OC4H9)4. The morphologies and crystal structures are characterized by SEM and XRD. The results indicate that netlike and plate-like Bi12TiO20 crystals can be synthesized using KOH and NaOH, respectively, both belonging to the cubic crystal system. Furthermore, the photocatalysis properties are characterized by the photodegradation of RhB under simulated sunlight illumination. The results show that the two Bi12TiO20 samples synthesized by hydrothermal method have enhanced photocatalysis properties comparing with those synthesized by solid-state reaction under visible light irradiation. The photodegradation rate of RhB with plate-like Bi12TiO20 crystals can reach 78.2 % after 180 min of illumination.
-
1 价值链管理概述
美国管理学家迈克·比特(michael Porter)在1985年针对产业问题提出了价值链分析理论。他认为:“企业提供给顾客的产品或服务,其实是由一连串的活动组合起来所创造出来的。每一种活动,都有可能促成最终产品的差异性,从而提升价值。”[1]也就是说,企业从取得原料、投入劳力、运用技术到转化为有价值的商品或服务会牵涉到许多活动,这些经营活动可分为几个阶段,而每一阶段对最终产品都有些贡献,也就是理论中所谓的价值链。每家公司都有自己的价值链,而企业的价值链同时会和供货商、厂商本身及顾客的价值链相连,构成一个产业的价值链(一个更大的价值链体系)。企业创造出这些价值,以价值链为分析的架构,思考如何在每一个企业价值活动上,寻找降低成本或创造差异的策略作为,同时进一步分析供货商、厂商与顾客三个价值链之间的联结关系,寻找可能的发展机会,也依赖这些价值获得利润得以生存。
企业管理的核心观念是降低成本并提高利润。原来管理者一直从产品本身的角度来考虑降低成本进而提高利润。成本产生于产品生产过程的各个环节,并在人流、物流、信息流、资金流中伴随着新价值的创造。因此,在价值链价值流中蕴含着更多的成本控制和利润提高机会,只有通过对企业的价值链和价值流进行分析,才能进行有效的企业管理。
价值链理论认为企业的价值增值过程,按照经济和技术的相对独立性,可以分为既相互独立又相互联系的多个价值活动,这些价值活动形成一个独特的价值链。笔者认为价值链可以分为两部分:
(1) 外部价值链
横向价值链主要反映同类产品在不同的生产者之间的价值运动过程,要充分考虑企业目前和潜在的竞争对手,争取获取竞争优势。横向价值链分析主要包括决策、预算和分析三个方面,企业要面临现实和潜在的竞争者,就不得不为了获得竞争优势而形成产品差异,努力降低成本。此外,企业要想方设法对竞争对手的产品特别是成本信息进行分析,从而提高产品成本方面的竞争力。
(2) 内部价值链
内部价值链分析指的是企业的内部价值运动。内部价值链分析始于原材料、外购件的采购,而终于产品的销售-顾客价值的实现。其目的是找出最基本的价值链、企业生产作业的成本动因及与竞争对手的成本差异,区分增值与非增值的作业,探索提高增值作业效率的途径。内部价值链分析涉及决策、预算、分析和控制所有方面,企业的内部价值链分析涉及企业的职能活动和生产经营活动。
目前,各个企业都在积极地寻找优化价值链的方法。价值链分析就是要通过从战略上对行业价值链进行分析以了解企业在行业价值链中所处的位置;通过企业内部价值链分析以了解自身的价值链;通过对竞争对手的价值链分析以了解自己所处的竞争环境;通过对杜会价值链的分析以了解企业与外部物质世界物质交换的价值关系。企业搏击于市场,其经营管理策略要从利润增长导向型管理转向价值导向型管理。价值导向型管理模式注重现金流、客户价值、经济增加值(或称价值链增值)。价值链管理不仅强调企业的各个供应链环节间的分工、协作、专业化,更应强调企业最高管理层对整个企业资源的监控与整合。进一步说,“价值链管理己经从单一企业个体扩展到个体外部整个供应链上的供应商和客户,进而形成了一个价值链联盟,出现了多赢的结果。”[2]企业管理的目标也由利润最大化发展成为价值增值最大化,价值链管理己成为企业经营管理的核心内容。
2 价值链管理的新趋势
2.1 现代信息技术引致全面价值链管理
价值链管理需要紧密结合信息技术,将价值链管理思想落实到企业的管理活动中,以实现价值增值的最大化,创造企业各方利益相关者的共赢。20世纪80年代后期,企业管理模式由纵向一体化发展成为横向一体化,这种基于价值链的横向管理模式可以使企业在最短时间里找到最好的合作伙伴,用最低的成本、最快的速度、最好的质量赢得市场,因此而受益的不仅仅是企业个体,而是企业群体。企业的概念己经从一个单一企业扩展到企业外部整个供应链上的供应商和客户。
在这种情况下,应用信息技术,扩大价值链管理的视野,企业可以利用现代计算机网络技术打破传统的时间和空间概念,有效地加快价值信息的交流和传输,与客户和供应商进行信息共享,协调生产,方便、快捷、高效地进行各种价值管理活动。借助于现代计算机信息技术,企业管理者只需分类设计与各业务职能部门的信息接口,就能够准确、及时地获取价值信息并进行加工处理,实现信息处理的动态化和实时化,并根据信息的不同特征,分类存储以备决策之用;引入供应链管理(SCM)、企业资源计划(ERP)、客户关系管理(CRM)等信息系统构建模型,借助网络技术,使企业生产经营过程中的物流、资金流、信息流有效集成并在价值链联盟中区别不同情况,在不同程度上实现共享。对企业经营活动的过程进行实时对比和实时分析。“充分、合理地应用现代信息技术的实时功能,及时了解企业内部各部门的信息,及其价值链上的供应商、客户的有关信息并作出相应决策,将工作重点放在更加富有挑战性的价值信息的分析、利用工作和价值链的控制和管理工作上。通过指导、调节、约束、促进等环节干预企业的经营业务,以实现提高经营效率和效益,从而达到价值增值的这一终极目标。”[3]
2.2 价值链的分解、整合与外包
在科学技术突飞猛进发展的今天,消费者的需求日益多样化,这就要求杜会分工更加细化,致使价值链的增值环节变得越来越多,结构也愈加复杂。一种产品的服务所形成的价值链过程己很少能由一家企业来完成,除非企业具有非常充分的资金和十分全面的能力。于是价值链就开始分解,一些新的企业加入了价值链,并在某个环节建立起新的竞争优势。这种竞争优势表现为在该环节上具有成熟、精湛的技术和较低的成本。它们的进入使一些大而全、小而全的企业在竞争中处于劣势,迫使它们不得不放弃某些价值环节,从自己的比较优势出发,选择若干环节培育并增强其竞争能力,重新确立自己的优势地位。价值链的不断分解,使市场上出现了许多相对独立的具有一定比较优势的增值环节。这些原本属于某个价值链的环节一旦独立出来,就未必只对应于某个特定的价值链,它也有可能加入到其他相关的价值链中去。于是出现了新的市场机会-价值链的整合。即可以设计一个新的价值链,通过市场选择最优的环节,把它们联结起来,创造出一个价值链。在生产能力相对过剩、市场竞争激烈的情况下,这种整合的机会也越来越多。
在不久的将来,企业将会越来越多地将价值链的非核心环节业务外包给其他企业,特别是中小型企业,这就是价值链的外包战略,它必将成为未来企业关注的热点。它可以有效地降低产品成本,引进和利用外部资源,有效地确立企业的竞争优势。从战略上看,业务外包可以给企业提供较大的灵活性,尤其是在购买高速发展的新技术、新式样的产品,或复杂系统的组成零部件方面更是如此。另外,当多个一流的供应商同时生产一个系统的组成部件时,就会降低外包企业的专有资产投资,缩短设计和生产周期。供应商既有相关方面的人才优势,又有专门领域的复杂的技术知识,而且可以不断地更新产品。企业实行价值链的外包战略,把其所研制技术和零部件所要承担的风险扩散到每个供应商身上,就无须承担零部件的研究与开发计划失败的全部风险,也不必为每一零部件系统投资或不断地扩大配件本身的生产能力。这样,企业就可以通过价值链的分解、整合与外包,全力改善本身核心业务的竞争能力。
2.3 价值链管理与会计管理渐渐融合
目前,会计管理经历着前所未有的挑战,这种挑战来自于会计信息外部使用者和内部使用者两方面的要求。从外部看,会计作为契约化的契约责任披露工具,会计信息相关性水平的降低,己经受到越来越多利益相关者的批评。会计信息使用者认为会计报告没有能够像人们期望的那样提供有价值的信息,会计信息严重不完整,会计信息缺乏相关性,现行财务会计报告只关注过去而不重视未来。会计信息的滞后性己经不能满足企业实时控制和多目标决策的要求。1986年,美国全国会计师协会(NAA)在波士顿召开了议肛为肛展望90年代成本会计”的会议,与会代表一致认为现行的管理会计方法己经不能适应变化了的时代要求,提出应该建立新的会计信息系统。会计管理活动论认为会计是人们从事的一种管理活动,会计工作是一种经营管理工作,会计部门是企业的一个经营管理部门,主张使用肛会计管理”概念,会计管理的内容被抽象为价值管理。正是因为会计具有管理功能,会计才能进入价值链管理体系,基于价值链管理的价值链会计才成为可能。也许将来价值链管理与会计管理渐渐融合形成众望所归的价值链会计管理。
与传统的企业管理以个别企业的内部管理为基础相适应,传统的会计体系同样基于单个企业和企业内部的价值活动,会计管理侧重于企业内部的价值管理,对企业核心竞争力有重要影响的企业外部价值活动关注不足,从而极大地限制了会计信息的决策作用。随着经济环境的变化,企业活动与外部环境的关系日趋密切,价值链对企业的影响越来越明显。上个世纪末,企业管理模式开始引入价值链管理模式,价值链管理自然而然被提到非常重要的位置,从而要求建立以价值链为中心的管理机制。这时作为价值管理活动的会计管理也就自然而然地关注企业价值链的活动,企业的会计活动从注重企业内部到同时注重外部合作关系,会计管理从内部价值管理向外部价值管理延伸,价值链会计的话肛就自然被提出来了。另一方面,客观杜会经济环境的变化,也为价值链会计的产生创造了条件,并使其发展成为可能。例如,IT技术的飞速发展,计算机在企业中的普及应用,为价值链会计提供了技术基础;价值链、数字价值链、虚拟价值链、价值网和价值中枢等理论的提出,为价值链会计提供了理论支持;现代管理会计的作业成本计算、作业成本管理等方法的应用,财务会计对自创商誉、衍生金融工具、人力资本等的确认和计量以及多层次彩色财务报告模式等问肛的讨论,为价值链会计提供了研究示范。
所谓价值链会计就是对企业价值信息及其背后深层次关系的研究,具体可表述为:是收集、加工、存储、提供并利用价值信息,实施对企业价值链的控制和管理,保证企业的价值链能够合规、高效、有序运转,从而为企业创造最大化的价值增值及其合理分配的一种管理活动;价值链会计的对象是价值链信息及其所体现的经济关系,其表现形式是价值链,载体包括资金流、信息流和实物流,实质是价值链信息背后所体现的经济关系;价值链会计的目的大体上可归纳为:疏通信息传递渠道、调整企业价值链,从而协调各部门、环节间的协作关系,为企业创造最大化的价值增值,即利用会计的特有功能与方法为企业价值增值最大化服务。因此,在时间维度上,价值链会计以会计实时控制为核心,沿着事前预算管理、事中实时控制和事后考评管理开展全方位、全过程的会计管理;在空间维度上,价值链会计把原来的以单一企业形式存在的会计核算主体扩展为以价值链联盟形式存在的全新形式的会计管理主体,同时,将以货币为计量手段的各会计核算对象扩展为以价值链形式存在的一切可以量化的会计管理对象。
3 价值链管理的现实思考
价值链管理,要靠现代信息技术实现。所以信息技术与会计核算(电算化软件)、财务管理软件(网络化)、全面预算管理以及企业资源计划(ERP)软件结合运用,以企业价值增值为核心,从顾客、分销商、合作伙伴、核心企业到供应商的所有环节,实现供应链联盟业务协同、信息共享,集中管理,体现协同和多赢的商业目标,实现从生产领域到流通领域一步到位的全业务过程管理和增值。利用价值链管理,可以使营销和物流环节得以完善和优化,从而建立敏捷互动的市场反应与控制能力,全面提升客户和伙伴的满意度。企业的价值链管理是现代经济的产物,始终处于不断的发展完善之中。随着我国经济的发展,它必将具有更加广阔的应用前景。
3.1 改革现存组织机构,构建统一的价值链管理信息平台
价值链管理应该建立统一的信息平台,通过平台实现价值链全程各个价值系统用户管理和认识的统一,实现各个价值系统入口的集中和统一;通过可控制内部、单元技术,实现个性化的系统定制,形成一个统一的用户交互界面;通过信息平台来实现不同业务系统的数据抽取和整合,进而实现数据交换的“枢纽”功能,满足管理和分析的需要。同时,在统一的信息平台基础上,实现企业内部的信息发布与共享,B常办公、决策支持、绩效管理等应用功能,构成企业办公管理平台。为适应价值链管理机制,对现存的组织机构要进行变革,以创造良好的支持系统。为了构建这个价值键管理信息平台,还要精简和关闭原有影响企业效益的业务,使组织机构趋于扁平化,提高工作效率,精干核心业务,成立急需的机构,进行业务研究创新。
3.2 优化企业内、外部价值链,要建立与价值链相适应的规章制度
在企业内部建立价值最大化的标准制度,建立以现金流量为基础,以经济增加值(EVA)为内容的绩效评价体系等,实现人事、财务、资源集中式管理,实现集团集中监控,实现集团规模经济。同时,优化外部价值链。建立以市场和客户需求为导向,以提高竞争力、市场占有率、客户满意度和获取企业价值最大化为目标,以协同商务、协同竞争和多赢原则为运作模式,通过运用现代企业管理思想、方法和信息技术、网络技术与集成技术,达到对整体价值链上的信息流、物流、资金流、商流、工作流的有效规划的控制。从而将核心企业与客户、分销商、供应商、服务商连成一个完整的网络结构,形成价值联盟的群体。
-
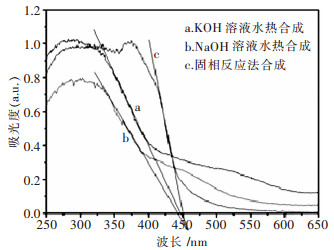
表 1 不同样品的最大吸收阈波长和禁带宽度
样品 最大吸收阈波长λg /nm 禁带宽度Eg /eV a 448 2.77 b 443 2.80 c 451 2.75 -
[1] Carey J H, Lawrence J, Tosine H M. Photodechlorination of PCB's in the presence of titanium dioxide in aqueous suspensions[J]. Bulletin of Environmental Contamination and Toxicology, 1976, 16(6): 697-701. doi: 10.1007/BF01685575
[2] Valant M, Suvorov D. Processing and dielectric properties of sillenite compounds Bi12MO20-δ(M=Si, Ge, Ti, Pb, Mn, B1/2P1/2)[J]. Journal of the American Ceramic Society, 2001, 84(12): 2900-2904. doi: 10.1111/jace.2001.84.issue-12
[3] Wei W, Dai Y, Huang B. First-principles characterization of Bi-based photocatalysts: Bi12TiO20, Bi2Ti2O7, and Bi4Ti3O12[J]. The Journal of Physical Chemistry C, 2009, 113(14): 5658-5663. doi: 10.1021/jp810344e
[4] Guo W, Zhang S, Guo Y, et al. Template-free and morphology-controlled hydrothermal growth of single-crystalline Bi12TiO20 with excellent simulated sunlight photocatalytic activity[J]. RSC Advances, 2013, 3(12): 4008-4017. doi: 10.1039/c3ra22592e
[5] Zhu X, Zhang J, Chen F. Study on visible light photocatalytic activity and mechanism of spherical Bi12TiO20 nanoparticles prepared by low-power hydrothermal method[J]. Applied Catalysis B: Environmental, 2011, 102(1): 316-322. http://www.sciencedirect.com/science/article/pii/S0926337310005503
[6] Xu S, Shangguan W, Yuan J, et al. Photocatalytic properties of bismuth titanate Bi12TiO20 prepared by co-precipitation processing[J]. Materials Science and Engineering: B, 2007, 137(1): 108-111. https://www.researchgate.net/publication/222316244_Photocatalytic_Properties_of_Bismuth_Titanate_Bi12TiO20_Prepared_by_Co-Precipitation_Processing
[7] Zhou J, Zou Z, Ray A K, et al. Preparation and characterization of polycrystalline bismuth titanate Bi12TiO20 and its photocatalytic properties under visible light irradiation[J]. Industrial & engineering chemistry research, 2007, 46(3): 745-749. https://www.researchgate.net/publication/231374471_Preparation_and_Characterization_of_Polycrystalline_Bismuth_Titanate_Bi12TiO20_and_Its_Photocatalytic_Properties_under_Visible_Light_Irradiation
[8] Morrison A D. Some properties of Bi12TiO20 and the system Bi2O3-TiO2[J] Ferroelectrics, 1971, 2(1): 59-62 doi: 10.1080/00150197108243946
[9] Yao W, Wang H, Xu X, et al. Photocatalytic property of bismuth titanate Bi12TiO20 crystals[J]. Applied Catalysis A: General, 2003, 243(1): 185-190. doi: 10.1016/S0926-860X(02)00564-1
[10] Yao W, Wang H, Xu X, et al. Photocatalytic property of Zn-doped Bi12TiO20[J]. Journal of Materials Science Letters, 2003, 22(14): 989-992. doi: 10.1023/A:1024777006505
[11] Yao W, Wang H, Xu X, et al. Characterization and photocatalytic properties of Ba doped Bi12TiO20[J]. Journal of Molecular Catalysis A: Chemical, 2003, 202(1): 305-311.
[12] Wei J, Huang B, Wang P, et al. Photocatalytic Properties of Nitrogen-Doped Bi12TiO20 Synthesized by Urea Addition Sol-Gel Method[J]. International Journal of Photoenergy, 2012, 2012: 135132
[13] Hou J, Qu Y, Krsmanovic D, et al. Solution-phase synthesis of single-crystalline Bi12TiO20 nanowires with photocatalytic properties[J]. Chemical Communications, 2009 (26): 3937-3939. doi: 10.1039/b906290d
[14] Hou J, Qu Y, Krsmanovic D, et al. Hierarchical assemblies of bismuth titanate complex architectures and their visible-light photocatalytic activities[J]. Journal of Materials Chemistry, 2010, 20(12): 2418-2423. doi: 10.1039/b923124b
[15] Hou J, Wang Z, Jiao S, et al. 3D Bi12TiO20/TiO2 hierarchical heterostructure: synthesis and enhanced visible-light photocatalytic activities[J]. Journal of hazardous materials, 2011, 192(3): 1772-1779. doi: 10.1016/j.jhazmat.2011.07.013
[16] Hou J, Cao R, Jiao S, et al. PANI/Bi12TiO20 complex architectures: Controllable synthesis and enhanced visible-light photocatalytic activities[J]. Applied catalysis. B, Environmental, 2011, 104(3/4): 399-406.
[17] Hou J, Jiao S, Zhu H, et al. Carbon-modified bismuth titanate nanorods with enhanced visible-light-driven photocatalytic property[J]. CrystEngComm, 2011, 13(14): 4735-4740. doi: 10.1039/c1ce05409k
[18] Guo W, Yang Y, Guo Y, et al. Self-assembled hierarchical Bi12TiO20-graphene nanoarchitectures with excellent simulated sunlight photocatalytic activity[J]. Physical Chemistry Chemical Physics, 2014, 16(6): 2705-2714. doi: 10.1039/c3cp53070a
[19] Tsai C, Yang C, Liao Y, et al. Hydrothermally grown bismuth ferrites: controllable phases and morphologies in a mixed KOH/NaOH mineralizer[J]. Journal of Materials Chemistry, 2012, 22(34): 17432-17436. doi: 10.1039/c2jm33859a
[20] Hagfeldt A, Graetzel M. Light-induced redox reactions in nanocrystalline systems[J]. Chemical Reviews, 1995, 95(1):49-68. doi: 10.1021/cr00033a003



 下载:
下载: